Hòa tan hoàn toàn m gam hỗn hợp gồm Al và Al2O3 trong 200 ml dung dịch HCl 2M, thu được 1,68 lít khí H2 và dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, kết quả thí nghiệm được ghi ở bảng sau:
| Thể tích dung dịch NaOH (ml) | 340 | 470 |
| Khối lượng kết tủa (gam) | 2a | a-0,78 |
A. 3,30.
B. 3,90.
C. 1,65.
D. 4,50.
Đáp án: B. 3,90.
Giải thích
BTe => nAl = 2/3.nH2 = 2/3.0,075 = 0,05 mol. Đặt nAl2O3 = x mol
Do hỗn hợp bị hòa tan hết => 3nAl3+ ≤ nCl- => nAl3+ ≤ 0,4/3 => mAl(OH)3 ≤ 10,4 gam
Mặt khác, ta thấy mAl(OH)3 tại V = 470ml < mAl(OH)3 tại V = 340 ml nên suy ra tại V = 470 ml thì Al(OH)3 đã bị hòa tan 1 phần.
Xét 2 trường hợp sau:
+ TH1: Tại V = 340 ml, Al(OH)3 bị hòa tan một phần
=> nNaOH (2) - nNaOH (1) = nAl(OH) (1) - nAl(OH)3 (2)
=> 0,47−0,34= \({2a \over 78}−{a−0,78 \over 78}\) => a = 9,36 => 2a = 18,72 gam không thỏa mãn mAl(OH)3 < 10,4 gam (loại)
+ TH2: Tại V = 340 ml, Al(OH)3 chưa bị hòa tan
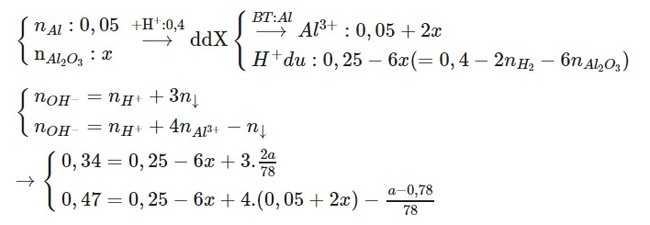
a = 3,12
x = 0,025
=>m = 0,05.27 + 0,025.102 = 3,9 gam
Câu hỏi liên quan
1. Hòa tan vừa hết 7 gam hỗn hợp X gồm Al và Al2O3 trong dung dịch NaOH đun nóng thì có 0,2 mol NaOH đã phản ứng, sau phản ứng thu được V lít khí H2 (đktc). Giá trị của V là
A. 5,60.
B. 4,48.
C. 2,24.
D. 3,36.
Đáp án: B. 4,48
Hòa tan Al và Al2O3 trong dung dịch NaOH đun nóng thì có 0,2 mol NaOH đã phản ứng, sau phản ứng thu được 4,48 lít khí H2 (đktc)
Xem giải thích đáp án câu 1 chi tiết tại đây: Hòa tan hỗn hợp Al và Al2O3 trong dung dịch NaOH đun nóng
2. Cho m gam hỗn hợp bột Al và Al2O3 tác dụng vừa đủ với dung dịch HCl, thu được dung dịch X và 0,672 lít H2 ở đktc. Nếu cho X tác dụng với 90 ml dung dịch NaOH 1M hoặc 130 ml dung dịch NaOH 1M thì đều thu được một lượng kết tủa như nhau. Giá trị của m là
A. 2,58.
B. 2,31.
C. 1,83.
D. 1,56.
Đáp án: D. 1,56.
Giải thích
Bảo toàn electron: 3nAl = 2nH2 ⇒ nAl = 0,02 mol.
"vừa đủ" ⇒ X chỉ chứa AlCl3 || 0,09 mol hay 0,13 mol NaOH cho cùng 1 lượng kết tủa
⇒ 0,09 mol NaOH thì kết tủa chưa đạt cực đại và 0,13 mol NaOH thì kết tủa bị hòa tan 1 phần.
⇒ nkết tủa = 0,09 ÷ 3 = 0,03 mol.
Mặt khác, khi bị hòa tan 1 phần thì:
\(n_{{OH}^–}\) = \(4n_{{Al}^{3+}}\) – nkết tủa ⇒ \(n_{{Al}^{3+}}\) = (0,03 + 0,13) ÷ 4 = 0,04 mol.
Bảo toàn nguyên tố Al: \(n_{Al_2O_3}\) = 0,01 mol
⇒ m = 1,56(g)
3. Hòa tan 21 gam hỗn hợp gồm Al và Al2O3 bằng HCl được dung dịch A và 13,44 lít H2(đktc). Thể tích dung dịch (lít) NaOH 0,5M cần cho vào dung dịch A để thu được 31,2 gam kết tủa là?
A. 2,4
B. 2,4 hoặc 4
C. 4
D. 1,2 hoặc 2
Đáp án: B. 2,4 hoặc 4
Trên đây là phương pháp giải bài tập hòa tan hoàn toàn m gam hỗn hợp Al Al2O3 trong 200ml dung dịch HCl 2M và các dạng bài tập liên quan. Ngoài tài liệu giải Hóa 12, các em có thể tham khảo các môn học khác trên Đọc Tài Liệu để ôn luyện toàn diện. Chúc các em học tốt!
