Bộ đề thi thử THPT Quốc gia 2020 môn Hóa mã đề 212 là đề thi tham khảo được Đọc Tài Liệu sưu tầm và biên soạn. Qua bộ đề sẽ giúp các em ôn tập kiến thức và rèn luyện kĩ năng giải đề thi thử môn hóa 2020.
Đề thi thử môn hóa 2020
Đề thi THPT Quốc gia 2020 môn Hóa mã đề 212 này gồm 40 câu hỏi trắc nghiệm được biên soạn theo đúng câu trúc đề thi chính thức của Bộ GD&ĐTvà nội dung theo sát chương trình học môn Hóa học lớp 12. Các em có thể làm bài thi online hoặc ghi đáp án từng câu ra giấy với thời gian làm bài là 50 phút rồi sau đó kiểm tra lại kết quả thi của mình qua phần đáp án ở phần cuối tài liệu này.
Có thể tải đề thi thử này về với 2 định dạng PDF hoặc DOC để in ra phía dưới!
Câu 1. Dung dịch A có \(\left[ {{H^ + }} \right] = {10^{ - 3}}\)M sẽ có môi trường
A. Trung tính.
B. Axit.
C. Bazơ.
D. Không xác định.
Câu 2. Cho dãy các chất sau: \(NaOH,{\rm{ }}HN{O_3}\),\({\rm{ }}Ba{\left( {OH} \right)_2}\),\({\rm{ }}HCl{O_4},{\rm{ }}C{H_3}COOH\),\({\rm{ }}N{H_3}\). Số axit, bazơ lần lượt là
A. 3 và 3.
B. 5 và 2.
C. 4 và 3.
D. 3 và 4.
Câu 3. Khí \({N_2}\) khá trơ ở nhiệt độ thường là do
A. N có bán kính nguyên tử nhỏ, phân tử \({N_2}\) không phân cựC.
B. Nguyên tử N có độ âm điện lớn nhất trong nhóm VA.
C. Trong phân tử \({N_2}\), mỗi nguyên tử còn 1 cặp electron chưa liên kết.
D. Trong phân tử \({N_2}\) chứa liên kết ba rất bền.
Câu 4. Trong các phản ứng sau, phản ứng nào \(N{H_3}\) không thể hiện tính khử?
A. \(4N{H_3} + 5{O_2} \to 4NO + 6{H_2}O\).
B. \(N{H_3} + HCl \to N{H_4}Cl\).
C. \(8N{H_3} + 3C{l_2} \to 6N{H_4}Cl + {N_2}\).
D. \(2N{H_3} + 3CuO \to 3Cu + 3{H_2}O + {N_2}\).
Câu 5. Nung nóng m gam bột sắt ngoài không khí, sau phản ứng thu được 36 gam hỗn hợp X gồm \(Fe,{\rm{ }}FeO\),\({\rm{ }}F{e_2}{O_3} và F{e_3}{O_4}\). Hòa tan hết X trong dung dịch \(HN{O_3}\) loãng thu được 5,6 lít hỗn hợp khí Y gồm \(NO và N{O_2}\) có tỉ khối so với \({H_2}\) là 19. Giá trị m là
A. 16.
B. 32.
C. 28.
D. 20.
Câu 6. Cacbon vô định hình và than chì là hai dạng thù hình của nhau vì
A. Có tính chất vật lí tương tự nhau.
B. Đều do nguyên tố cacbon tạo nên.
C. Có cấu tạo mạng tinh thể giống nhau.
D. Chúng có tính chất hoá học không giống nhau.
Câu 7. Dẫn hơi nước qua than nóng đỏ thì thu được V lít (đktc) hỗn hợp khí X gồm \(C{O_2}, CO, {H_2}\); tỉ khối hơi của X so với \({H_2}\)
là 7,8. Cho toàn bộ V lít hợp khí X ở trên khử vừa đủ 24 gam hỗn hợp \(CuO, F{e_2}{O_3}\) nung nóng, thu được rắn Y chỉ có 2 kim loại. Cho toàn bộ Y vào dung dịch HCl dư thấy có 4,48 lít \({H_2}\) bay ra (đktc). Giá trị của V làA. 10,08.
B. 11,20.
C. 13,44.
D. 8,96.
Câu 8. Ankan Y phản ứng với clo tạo ra 2 dẫn xuất monoclo có tỉ khối hơi so với \({H_2}\) bằng 39,25.
Tên của Y là
A. Butan.
B. Propan.
C. iso-butan.
D. 2-metylbutan.
Câu 9. Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích \({O_2}\), còn lại là \({N_2}\)) được khí \(C{O_2}, {H_2}O và {N_2}\). Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch \(Ba{\left( {OH} \right)_2}\) dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết \({d_{X/{O_2}}} < 2\). Công thức phân tử của X là
A. \({C_2}{H_7}N.\)
B. \({C_2}{H_8}N\).
C. \({C_2}{H_7}{N_2}\).
D. \({C_2}{H_4}{N_2}\).
Câu 10. Nung nóng 100 gam hỗn hợp gồm \(N{a_2}C{O_3}\) và \(NaHC{O_3}\) cho đến khối lượng không đổi còn lại 69 gam chất rắn. Thành phần % khối lượng mỗi chất trong hỗn hợp ban đầu là
A. 63% và 37%.
B. 84% và 16%.
C. 42% và 58%.
D. 21% và 79%.
Câu 11. Dẫn luồng khí CO qua hỗn hợp \(A{l_2}{O_3},{\rm{ }}CuO\),\({\rm{ }}MgO,{\rm{ }}F{e_2}{O_3}\) (nóng) sau khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm
A. \(A{l_2}{O_3},{\rm{ }}Cu,{\rm{ }}Mg,{\rm{ }}Fe.\)
B. \(Al,{\rm{ Fe,}}Cu,{\rm{ }}Mg.\)
C. \(A{l_2}{O_3},{\rm{ }}Cu,MgO,Fe\) .
D. \(A{l_2}{O_3},{\rm{ }}F{e_2}{O_3},{\rm{ }}Cu,{\rm{ }}MgO.\)
Câu 12. Có hai dung dịch, mỗi dung dịch đều chứa hai cation và hai anion không trùng nhau trong các ion sau:
\({K^ + }:0,15{\rm{ }}mol\), \(M{g^{2 + }}{\rm{: 0,1 mol, }}\)\(NH_4^ + :0,25{\rm{ }}mol;{\rm{ }}{H^ + }:0,2{\rm{ }}mol\);\({\rm{ }}C{l^ - }:0,1{\rm{ }}mol;{\rm{ }}SO_4^{2 - }:0,075{\rm{ }}mol\);\({\rm{ }}NO_3^ - :0,25{\rm{ }}mol\)
A. \({K^ + },{\rm{ }}M{g^{2 + }}\),\({\rm{ }}SO_4^{2 - },{\rm{ }}C{l^ - }\).
B. \({K^ + },{\rm{ }}NH_4^ + \),\({\rm{ C}}O_3^{2 - },{\rm{ }}C{l^ - }\).
C. \(NH_4^ + ,{\rm{ }}{H^ + }\),\({\rm{ }}NO_3^ - ,{\rm{ }}SO_4^{2 - }\).
D. \(M{g^{2 + }},{\rm{ }}{{\rm{H}}^ + }\),\({\rm{ }}SO_4^{2 - },{\rm{ }}C{l^ - }\).
Câu 13. Loại thuỷ tinh khó nóng chảy chứa 18,43% \({K_2}O\); 10,98% \(CaO\) và 70,59% \(Si{O_2}\) có công thức dưới dạng các oxit là
A. \({K_2}O.CaO.4Si{O_2}\).
B. \({K_2}O.2CaO.6Si{O_2}\).
C. \({K_2}O.CaO.6Si{O_2}\).
D. \({K_2}O.3CaO.8Si{O_2}\).
Câu 14. Trong các phản ứng của Si với \(C{l_2},{\rm{ }}{F_2},{\rm{ }}{O_2},{\rm{ }}HN{O_3}\) đặc nóng, dung dịch NaOH, Mg. Số phản ứng mà trong đó Si thể hiện tính oxi hóa là
A. 5.
B. 4.
C. 3.
D. 1.
Câu 15. Oxi hoá hết 2,2 gam hỗn hợp hai ancol đơn chức thành anđehit cần vừa đủ 4,8 gam CuO. Cho toàn bộ lượng anđehit trên tác dụng với lượng dư dung dịch \(AgN{O_3}\)
trong \(N{H_3}\), thu được 23,76 gam Ag. Hai ancol lần lượt là :A. \(C{H_3}OH,{\rm{ }}{C_2}{H_5}C{H_2}OH.\)
B. \(C{H_3}OH,{\rm{ }}{C_2}{H_5}OH.\)
C. \({C_2}{H_5}OH,{\rm{ }}{C_3}{H_7}C{H_2}OH.\)
D. \({C_2}{H_5}OH,{\rm{ }}{C_2}{H_5}C{H_2}OH.\)
Câu 16. Thực hiện các thí nghiệm sau đây:
(1) Sục khí \({C_2}{H_4}\) vào dung dịch \(KMn{O_4}\).
(2) Cho \(NaHC{O_3}\) vào dung dịch \(C{H_3}COOH\).
(3) Chiếu sáng hỗn hợp khí metan và clo.
(4) Cho glucozơ tác dụng với \(Cu{\left( {OH} \right)_2}\) ở điều kiện thường.
(5) Đun etanol với \({H_2}S{O_4}\) đặc ở \(140^\circ C\).
(6) Đun nóng hỗn hợp triolein và hiđro (với xúc tác Ni).
(7) Cho phenol tác dụng với dung dịch NaOH.
(8) Cho anilin tác dụng với dung dịch brom.
(9) Cho metyl amin tác dụng với dung dịch \(FeC{l_3}\).
(10) Cho glixerol tác dụng với NA.
Những thí nghiệm xảy ra phản ứng oxi hoá - khử là
A. 5.
B. 3.
C. 4.
D. 6.
Câu 17. Este X đơn chức tác dụng với NaOH đun nóng thu được muối Y có công thức phân tử là \({C_3}{H_5}{O_2}Na\) và rượu \({Y_1}\). Oxi hóa \({Y_1}\) bằng CuO nung nóng thu được anđehit \({Y_2}\). \({Y_2}\) tác dụng với \(A{g_2}O\) dư, đun nóng thu được số mol Ag gấp 4 lần số mol \({Y_2}\). Vậy tên gọi của X là
A. etyl propionat
B. metyl propionat.
C. metyl axetat.
D. propyl propionat.
Câu 18. Dung dịch X chứa 0,01 mol \(Cl{H_3}N - C{H_2} - COOH\); 0,02 mol \(C{H_3} - CH\left( {N{H_2}} \right) - COOH\); 0,05 mol \(HCOO{C_6}{H_5}\). Cho dung dịch X tác dụng với 160 ml dung dịch KOH 1M đun nóng để phản ứng xảy ra hoàn toàn. Cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan. Giá trị của m là
A. 16,335 gam.
B. 8,615 gam.
C. 12,535 gam.
D. 14,515 gam.
Câu 19. Trung hoà hoàn toàn 8,88 gam một amin (bậc một, mạch cacbon không phân nhánh) bằng axit HCl, tạo ra 17,64 gam muối. Amin có công thức là
A. \({H_2}NC{H_2}C{H_2}C{H_2}C{H_2}N{H_2}\).
B. \(C{H_3}C{H_2}C{H_2}N{H_2}\).
C. \({H_2}NC{H_2}C{H_2}N{H_2}\).
D. \({H_2}NC{H_2}C{H_2}C{H_2}N{H_2}\).
Câu 20. Phát biểu nào sau đây không đúng?
A. Tinh bột là polime có cấu trúc dạng mạch phân nhánh và không phân nhánh.
B. Tinh bột không tan trong nước lạnh. Trong nước nóng từ \(65^\circ C\) trở lên, tinh bột chuyển thành dung dịch keo nhớt.
C. Tinh bột không phản ứng với dung dịch \({H_2}S{O_4}\) loãng, đun nóng.
D. Etanol có thể được sản xuất bằng phương pháp lên men các nông sản chứa nhiều tinh bột.
Câu 21. Thủy phân hoàn toàn 7,02 gam hỗn hợp X gồm glucozơ và saccarozơ trong dung dịch \({H_2}S{O_4}\) thu được dung dịch Y. Trung hòa hết lượng axit dư trong dung dịch Y rồi cho phản ứng ứng hoàn toàn với lượng dư dung dịch \(AgN{O_3}\) trong \(N{H_3}\) thì thu được 8,64 gam Ag. Thành phần % về khối lượng của saccarozơ trong hỗn hợp X là
A. 97,14%.
B. 24,35%.
C. 12,17%.
D. 48,71%.
Câu 22. Tiến hành hai thí nghiệm sau:
- Thí nghiệm 1:
Bước 1: Cho vào ống nghiệm 1 giọt dung dịch \(CuS{O_4}\) bão hòa + 2 ml dung dịch NaOH 30%.
Bước 3: Thêm khoảng 4 ml lòng trắng trứng vào ống nghiệm, dùng đũa thủy tinh khuấy đều.
- Thí nghiệm 2:
Bước 1: Lấy khoảng 4 ml lòng trắng trứng cho vào ống nghiệm.
Bước 2: Nhỏ từng giọt khoảng 3 ml dung dịch \(CuS{O_4}\) bão hòA.
Bước 3: Thêm khoảng 5 ml dung dịch NaOH 30% và khuấy đều.
Phát biểu nào sau đây sai?
A. Các phản ứng ở các bước 3 xảy ra nhanh hơn khi các ống nghiệm được đun nóng.
B. Sau bước 3 ở cả hai thí nghiệm, hỗn hợp thu được sau khi khuấy xuất hiện màu tím.
C. Sau bước 2 ở thí nghiệm 2, xuất hiện kết tủa màu xanh.
D. Sau bước 1 ở thí nghiệm 1, trong ống nghiệm xuất hiện kết tủa màu xanh.
Câu 23. Cho các polime sau: Tơ tằm, tơ visco, tơ axetat, tơ nitron, cao su buna-S, poli vinylclorua, poli vinylaxetat, nhựa novolac. Số polime có chứa nguyên tố oxi trong phân tử là
A. 4.
B. 5.
C. 3.
D. 6.
Câu 24. Cho m gam hỗn hợp X gồm Na và K (tỉ lệ mol 1:1) vào 500 ml dung dịch chứa hỗn hợp gồm \(A{l_2}{\left( {S{O_4}} \right)_3} 0,5M\)
và \({H_2}S{O_4} 1M\) sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Cho dung dịch Y tác dụng với 1,5 lít dung dịch HCl 1M, sau khi phản ứng xảy ra hoàn toàn thu được 23,4 gam kết tủa. Giá trị nhỏ nhất của m làA. 130,2 gam.
B. 27,9 gam.
C. 105,4 gam.
D. 74,4 gam.
Câu 25. Nhúng một thanh Al nặng 20 gam vào 400 ml dung dịch \(CuC{l_2}\) 0,5M. Khi nồng độ dung dịch \(CuC{l_2}\) giảm 25% thì lấy thanh Al ra khỏi dung dịch, giả sử tất cả Cu thoát ra bám vào thanh Al. Khối lượng thanh Al sau phản ứng là
A. 21,15 gam.
B. 21,88 gam.
C. 22,02 gam.
D. 22,3 gam.
Câu 26. Điện phân 100 ml dung dịch \(CuS{O_4} 0,2M\) với cường độ dòng điện 9,65A. Biết hiệu suất điện phân là 100%. Khối lượng Cu bám vào catot khi thời gian điện phân \({t_1} = 200\left( s \right) và {t_2} = 500\left( s \right)\) là
A. 0,32 gam và 0,64 gam.
B. 0,64 gam và 1,62 gam.
C. 0,64 gam và 1,28 gam.
D. 0,64 gam và 3,25 gam.
Câu 27. Cho 2 phản ứng sau:
(1) \(Cu + 2Fe{{Cl}_3} \rightarrow Cu{{Cl}_2} + 2Fe{{Cl_2}}\)
(2) \(Fe + Cu{{Cl}_2} \rightarrow Fe{{Cl}_2} + Cu\)
Kết luận nào dưới đây là đúng?
A. Tính oxi hoá của \(C{u^{2 + }} > F{e^{3 + }} > F{e^{2 + }}\).
B. Tính oxi hoá của \(F{e^{3 + }} > C{u^{2 + }} > F{e^{2 + }}\).
C. Tính khử của \(Cu > F{e^{2 + }} > Fe\).
D. Tính khử của \(F{e^{2 + }} > Fe > Cu\).
Câu 28. Hoà tan một lượng Fe vào dung dịch \({H_2}S{O_4}\) loãng thấy thoát ra \({V_1}\) , lít khí \({H_2}\). Mặt khác nếu hoà tan cùng một lượng Fe trên vào dung dịch \({H_2}S{O_4}\) đặc nóng thấy thoát ra \({V_2}\) lít khí \(S{O_2}\) (các thể tích đo ở cùng điều kiện). Mối quan hệ giữa \({V_1}\) và \({V_2} \)là
A. \({V_1} = 2{V_2}\).
B. \(2{V_1} = {V_2}\).
C. \({V_1} = {V_2}\).
D. \(3{V_1} = 2{V_2}\).
Câu 29. Nung m gam bột sắt trong oxi, thu được 4,5 gam hỗn hợp chất rắn X. Hòa tan hết hỗn hợp X trong dung dịch \({H_2}S{O_4}\)
đặc nóng (dư) thoát ra 1,26 lít (đktc) \(S{O_2}\) (là sản phẩm khử duy nhất).Giá trị của m là
A. 3,78.
B. 2,22.
C. 2,52.
D. 2,32.
Câu 30. Cho m gam hỗn hợp bột X gồm \(F{e_x}{O_y}, CuO và Cu\) (x, y nguyên dương) vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch \(AgN{O_3}\), thu được 102,3 gam kết tủA. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 22,7.
B. 34,1.
C. 29,1.
D. 27,5.
Câu 31. Cho hình sau:
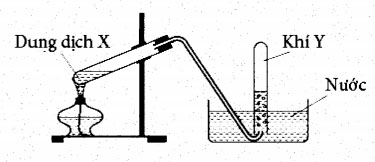
Hình vẽ trên mô tả thí nghiệm điều chế khí nào sau đây
A. \({C_2}{H_2}.\)
B. \(C{H_4}\).
C. \({C_2}{H_4}\).
D. \(N{H_3}\).
Câu 32. Trong khi làm các thí nghiệm ở lớp hoặc trong các giờ thực hành hóa học có một số khí thải: \(C{l_2},{\rm{ }}{H_2}S\),\({\rm{ }}S{O_2}\),\({\rm{ }}N{O_2},{\rm{ }}HCl\). Biện pháp đúng dùng để khử các khí trên là
A. Dùng bông tẩm giấm ăn nút ngay ống nghiệm sau khi đã quan sát hiện tượng.
B. Sục khí vào cốc đựng thuốc tím hoặc bông tẩm thuốc tím nút ngay ống nghiệm sau khi đã quan sát hiện tượng.
C. Dùng bông tẩm xút hoặc nước vôi trong nút ngay ống nghiệm sau khi đã quan sát hiện tượng.
D. Sục khí vào cốc đựng nước.
Câu 33. Tiến hành điện phân 100g dung dịch chứa \(AlC{l_3}\) (7x mol) và \(FeC{l_2}\) (10x mol) (có màng ngăn) với cường độ dòng điện 5A, khối lượng dung dịch trong quá trình điện phân thay đổi theo thời gian được biểu diễn bằng đồ thị sau:
Khi điện phân tới thời điểm \(2,5{t_1}\) giây khi khí bắt đầu thoát ra tại catot thì tạm dừng điện phân, sau thêm một lượng dung dịch \(N{a_2}S{O_4}\) vào rồi điện phân tiếp tới thời điểm 17370 giây thì kết thúc quá trình điện phân, lấy màng ngăn ra; để yên dung dịch một thời gian thì khối lượng dung dịch còn lại m gam.
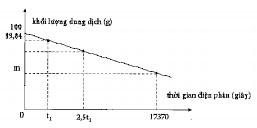
Giá trị của m là
A. 47,63 gam.
B. 28,56 gam.
C. 33,37 gam.
D. 44,75 gam.
Câu 34. Cho 31,15 gam hỗn hợp bột Zn và Mg (tỷ lệ mol 1 : 1) tan hết trong dung dịch hỗn hợp gồm \(NaN{O_3}\) và \(NaHS{O_4}\) thu được dung dịch A chỉ chứa m gam hỗn hợp các muối và 4,48 lít (đktc) hỗn hợp khí B gồm \({N_2}O\) và \({H_2}\). Khí B có tỷ khối so với \({H_2}\) bằng 11,5. m gần giá trị nào nhất?
A. 240.
B. 255.
C. 132.
D. 252.
Câu 35. Cho các phát biểu sau:
(a) Khi nấu canh cua thì thấy các mảng “riêu cua” nổi lên là do sự đông tụ của protein do nhiệt độ.
(b) Dầu ăn và mỡ bôi trơn có cùng thành phần nguyên tố.
(c) Cao su có tính đàn hồi, không dẫn điện, không dẫn nhiệt.
(d) Muối mono natri của axit glutamic được dùng làm mì chính.
(e) Khi ăn cơm, nếu nhai kĩ sẽ thấy có vị ngọt là do tinh bột trong cơm bị thủy phân thành glucozơ.
(g) Khi bị ong đốt, để giảm đau nhức có thể bôi vôi tôi vào vết đốt.
Số phát biểu đúng là
A. 2.
B. 3.
C. 4.
D. 5.
Câu 36. Tiến hành các thí nghiệm sau:
(a) Cho dung dịch HCl vào dung dịch \(Fe{\left( {N{O_3}} \right)_2}\).
(b) Cho kim loại Be vào \({H_2}O\).
(c) Cho kim loại Al vào dung dịch \(HN{O_3}\) loãng nguội.
(d) \(N{O_2}\) tác dụng với nước có mặt oxi.
(e) Clo tác dụng sữa vôi \((30^\circ C)\).
(g) Lấy thanh Fe ngâm trong dung dịch \({H_2}S{O_4}\)
Số thí nghiệm có phản ứng oxi hóa - khử xảy ra là
A. 4.
B. 3.
C. 5.
D. 6.
Câu 37. Cho X, Y là hai axit cacboxylic đơn chức mạch hở \(\left( {{M_X} < {M_Y}} \right)\); T là este hai chức tạo bởi X, Y và một ancol no mạch hở Z. Đốt cháy hoàn toàn 6,88 gam hỗn hợp E gồm X, Y, T bằng một lượng vừa đủ \({O_2}\), thu được 5,6 lít \(C{O_2}\) (đktc) và 3,24 gam nước. Mặt khác 6,88 gam E tác dụng với dung dịch \(AgN{O_3}{\rm{/ }}N{H_3}\) dư thu được 12,96 gam Ag. Khối lượng rắn khan thu được khi cho cùng lượng E trên tác dụng với 150 ml dung dịch KOH 1M là
A. 10,54 gam.
B. 14,04 gam.
C. 12,78 gam.
D. 13,66 gam.
Câu 38. Cho hỗn hợp X gồm 3 este đơn chức. Đem đốt cháy m gam X thì cần vừa đủ 0,465 mol \({O_2}\) sản phẩm cháy thu được chứa x mol \(C{O_2}\). Thủy phân m gam X trong 90 ml dung dịch NaOH 1M (vừa đủ) thì thu được được 8,86 gam hỗn hợp muối Y và một ancol Z no đơn chức, mạch hở. Đem đốt cháy hoàn toàn hỗn hợp muối Y thì cần dùng 7,392 lít (đktc) khí \({O_2}\)
. Giá trị x làA. 0,38.
B. 0,14.
C. 0,34.
D. 0,46.
Câu 39. Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
| Mẫu thử | Thuốc thử | Hiện tượng |
| X | Qùy tím | Quỳ tím hóa đỏ |
| Y | \(Cu{\left( {OH} \right)_2}\) | Dung dịch xanh lam |
| X,Z | Dung dịch \(AgN{O_3}\) trong \(N{H_3}\) dư, đun nóng | Kết tủa Ag trắng sáng |
| T | Nước \(B{r_2}\) | Kết tủa trắng |
Các dung dịch X, Y, Z, T lần lượt là:
A. Phenol, etylen glicol, anđehit axetic , axit focmic.
B. Axit axetic, etylen glicol, anđehit axetic, phenol.
C. Axit focmic, glixerol, anđehit axetic, phenol.
D. Axit axetic, etylen glicol, anđehit axetic, phenol.
Câu 40. Cho hỗn hợp X gồm hai chất hữu cơ có cùng công thức phân tử \({C_2}{H_7}N{O_2}\) tác dụng vừa đủ với dung dịch NaOH đun nóng, thu được dung dịch Y và 4,48 lít hỗn hợp Z (ở đktc) gồm hai khí (đều làm xanh giấy quỳ ẩm). Tỉ khối hơi của Z đối với \({H_2}\)
bằng 13,75. Cô cạn dung dịch Y thu được khối lượng muối khan làA. 16,5 gam.
B. 14,3 gam.
C. 8,9 gam.
D. 15,7 gam.
Đáp án đề thi thử Hóa THPT QG 2020
| 1-B | 2-A | 3-D | 4-B | 5-C | 6-B | 7-B | 8-B | 9-A | 10-B |
| 11-C | 12-B | 13-C | 14-D | 15-A | 16-A | 17-B | 18-A | 19-D | 20-C |
| 21-D | 22-C | 23-B | 24-C | 25-D | 26-C | 27-B | 28-D | 29-A | 30-C |
| 31-C | 32-C | 33-A | 34-A | 35-C | 36-A | 37-C | 38-A | 39-C | 40-B |
Trên đây là bộ đề thi thử thpt quốc gia 2020 môn Hóa có đáp án Mã đề 212 giúp các em ôn tập lại các kiến thức đã học, đánh giá năng lực làm bài của mình và chuẩn bị cho kì kiểm tra THPT sắp tới được tốt hơn với số điểm cao như mong muốn.
Chúc các em thi tốt!