Đọc Tài Liệu giới thiệu chi tiết đề thi tuyển sinh vào lớp 10 môn Hóa năm học 2019 - 2020 trường THPT chuyên Lê Hồng Phong được cập nhật nhanh nhất giúp bạn tham khảo.

Đề thi Hóa vào 10 trường THPT chuyên Lê Hồng Phong năm 2019
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO NAM ĐỊNH ĐỀ CHÍNH THỨC |
ĐÊ THI TUYỂN SINH LỚP 10 TRƯỜNG THPT CHUYÊN NĂM HỌC 2019-2020 MÔN THI: HOÁ HỌC (Đề chuyên) Thời gian làm bài: 150 phút. |
Cho biết nguyên tử khối của: H= 1; C= 12; O = 16; Na = 23; Ca = 40.
Câu 1
1. Bằng phân tích hóa học, người ta tìm được các công thức thực nghiệm sau: H2C2PO4,H2C2O6Fe, H9O4N2P, H6C4O4Ba. Hãy đề xuất một chất phù hợp cho mỗi công thức thực nghiệm trên và gọi tên.
2. Đun nóng 100 gam dung dịch Na2CO3 bão hòa và hòa tan thêm 2 gam Na2CO3 vào. Sau khi để nguội dung dịch đến nhiệt độ ban đầu, thì thấy tách ra 8,6 gam chất X (rắn).
Biết rằng trong X, Na chiếm 16,084% theo khối lượng.
a. Xác định công thức của X.
b. Xác định nồng độ % của Na2CO3 trong dung dịch bão hòa.
c. Xác định độ tan của X.
3. Tiến hành hai thí nghiệm sau:
Thí nghiệm 1: hấp thụ hết V lít khí CO2 (đktc) vào dung dịch chứa 0,3 mol Ca(OH)2, sau khi các phản ứng xảy ra hoàn toàn, thu được m gam chất rắn.
Thí nghiệm 2: hấp thụ hết V lít khí CO2 (đktc) vào dun gdichj chứa 0,3 mol Ca(OH)2 vào 0,1 mol NaOH, sau khi các phản ứng xảy ra hoàn toàn, thu được 2m gam chất rắn. Xác định giá trị của V và m.
Câu 2
1. Viết các phương trình phản ứng xảy ra trong các thí nghiệm sau:
a. Cho dung dịch Na2CO3 vào dung dịch FeCl3, thu được kết tủa nâu đỏ và có khí thoát ra.
b. Cho dung dịch NaAlO2 vào dung dịch AlCl3, chỉ xuất hiện kết tủa trắng dạng keo.
2. Chất Z là muối của axit photphoric. Cho a mol NaOH vào dung dịch chứa a mol muối
Z, thu được dung dịch E chứa hai muối có số mol bằng nhau. Mặt khác, cho a mol HCl vào dung dịch chứa a mol muối Z, thu được dung dịch F chứa hai chất tan có số mol bằng nhau. Lập luận để xác định công thức phù hợp của Z và viết các phương trình hóa học của các phản ứng.
3. Hoàn thành các phản ứng hóa học theo sơ đồ chuyển hóa sau:
a. \(Fe + H2O \overset {t⁰} \rightarrow X1 + H2 \)
b. \(FeO + H2O \overset {t⁰} \rightarrow X1 + H2 \)
c. \(FeO+ H2 \overset {t⁰} \rightarrow X1 + H2O \)
d. X1 + H2SO4 → X2 + X3 + H2O
e. Fe2O3 + H2SO4 → X2 + H2O
f. X2 + NaOH → X4↓ + X5
Biết rằng: X1 là một oxit của sắt.
Xác định các chất trong sơ đồ chuyển hóa và viết các phương trình hóa học.
4. Chất A là hidroxit của sắt. Nung A trong điều kiện không có không khí, thu được chất rắn B là một oxit và hỗn hợp D gồm hai khí (ở nhiệt độ 127⁰C và áp suất 1 atm). Hỗn hợp D có tỉ khối so với H2 là 19/3. Xác định công thức của A và B. Biết nước bay hơi ở nhiệt độ 1000C và áp suất 1 atm.
Câu 3.
Trong các phân tử, liên kết đơn là sự dùng chung 1 cặp electron ; liên kết đôi là sự dùng chung 2 cặp electron và liên kết ba là sự dùng chung 3 cặp electron giữa hai nguyên tử. Công thức biểu diễn trật tự sắp xếp của các nguyên tử trong phân tử bằng các đường nối được gọi là công thức cấu tạo.
1. Biểu diễn công thức cấu tạo của các chất sau : C2H4, C2H2.
2. Trong các phân tử, các nguyên tử sẽ phân bố trong không gian sao cho sự đẩy lẫn nhau giữa các liên kết của cùng một nguyên tử là nhỏ nhất. Công thức tương ứng với sự phân bố đó được gọi là cấu trúc phân tử.
a. Giải thích tại sao các liên kết lại có sự đẩy lẫn nhau.
b. Biểu diễn cấu trúc phân tử của phân tử C2H4, C2H2.
3. Theo lý thuyết hiện đại về liên kết hóa học, liên kết đơn được coi là liên kết xichma (kí hiệu là ẟ), liên kết đôi gồm có 1 liên kết ẟ và 1 liên kết pi (kí hiệu làπ), liên kết ba gồm 1 liên kết ẟ và 2 liên kết π. Phản ứng tách đồng thời H2O và H2 của etanol (C2H5OH) khi có mặt xúc tác Cr2O3/Al2O3 ở 450⁰C tạo ra hidrocacbon X có thành phần 88,89% cacbon, phân tử khối của X nhỏ hơn 108. Trong cấu tạo của X, các liên kết π nằm cách nhau một liên kết ẟ.
a. Xác định công thức cấu tạo của X.
b. Viết phương trình phản ứng điều chế X từ etanol.
c. Các chất Y, Z, T là các đồng phân cấu tạo của X ; trong đó Y có nhiều liên kết π nhất có thể, Z không có liên kết π và T có một liên kết π duy nhất. Lựa chọn một công thức cấu tạo phù hợp với Y, Z, T.
Câu 4.
1. Chất béo là gì ? Khi để lâu trong không khí, chất béo thường có mùi ôi. Hãy cho biết nguyên nhân và cách hạn chế hiện tượng này.
2. Thực hiện phản ứng giữa axit axetic với rượu etylic bằng cách đun nóng hỗn hợp gồm axit axetic, rượu etylic và axit sunfuric 98%.
a. Viết phương trình hóa học của phản ứng xảy ra.
b. Sau phản ứng, hỗn hợp thu được gồm axit axetic, rượu etylic, etyl axetat, H2SO4 và nước. Trình bày cách để thu được etyl axetat.
3. Hợp chất hữu cơ X có \(Mx < 200\). Tỉ lệ khối lượng của các nguyên tố trong X là mC : mH : mO = 36 : 5 : 40. Khi cho X tác dụng với Na dư hoặc NaHCO3 dư đều cho số mol khí bằng số mol X đã phản ứng. Mặt khác, X tác dụng với NaOH trong dung dịch theo tỉ lệ mol 1 : 2, thu được dung dịch chỉ chứa một muối.
a. Viết các công thức cấu tạo có thể có của X.
b. Đun nóng X trong điều kiện thích hợp, thu được hợp chất Y, Y không tác dụng với Na nhưng phản ứng với NaOH theo tỉ lệ mol 1 : 2. Viết công thức cấu tạo của Y và các phương trình phản ứng xảy ra.
4. Ngưng tụ hai hoặc nhiều phân tử axit aminoaxetic (H2NCH2COOH) bằng cách tách H2O từ -OH của nhóm –COOH trong phân tử axit aminoaxetic này với –H của nhóm – NH2 trong phân tử axit aminoaxetic khác, người ta thu được các sản phẩm hữu cơ.
Đề thi tuyển sinh lớp 10 môn Hóa năm 2019 - THPT Chuyên Lê Hồng Phong đã được cập nhật tại bài viết này. Mời các bạn cùng chú ý theo dõi
Đáp án đề thi vào 10 năm 2019 môn Hoá chuyên trường Lê Hồng Phong - Nam Định
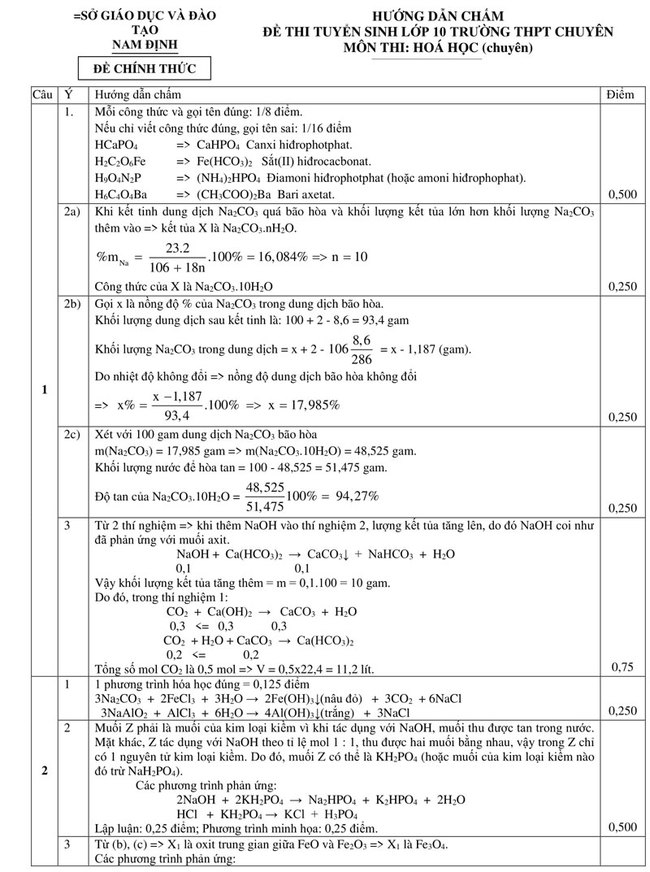


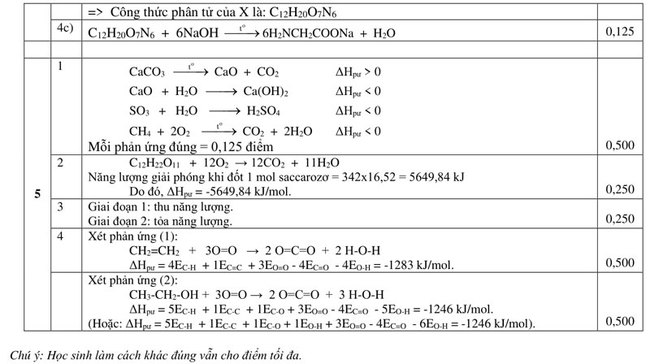
Xem thêm: Đáp án đề thi tuyển sinh vào lớp 10 môn văn chuyên Lê Hồng Phong - Nam Định 2019
Hi vọng với đáp án đề thi tuyển sinh lớp 10 môn Hoá chuyên năm 2019 của trường Lê Hồng Phong, Nam Định sẽ giúp các em có được kĩ năng trả lời câu hỏi, phân phối thời gian làm bài sao cho hợp lí để chinh phục đề thi sắp tới.