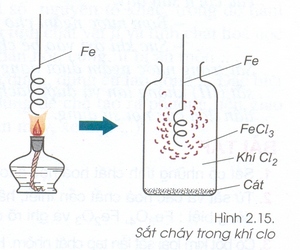
Cho dây sắt quấn hình lò xo (đã được nung nóng đỏ) vào lọ đựng khí clo. Sắt cháy sáng tạo thành khói màu nâu đỏ. Sắt đă phản ứng với khí clo tạo thành sắt (III) clorua. Trong phản ứng này, 2 nguyên tử sắt (Fe) tác dụng với 3 phân tử clo (Cl2) để tạo ra 2 phân tử FeCl3. Vì vậy hai chất Fe Cl2 khi phản ứng sẽ tạo ra muối sắt (III) clorua.
Phương trình phản ứng viết sai là Fe+Cl2$\overset {t^0} \rightarrow$FeCl2 sửa lại thành: 2Fe+3Cl2$\overset {t^0} \rightarrow$FeCl3