Đề bài
Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl. Phản ứng xong, thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học;
b) Tính khối lượng mạt sắt đã tham gia phản ứng
c) Tìm nồng độ mol của dung dịch HCl đã dùng.
Hướng dẫn giải
a) PTHH: Fe + 2HCl → FeCl2 + H2
b) Dựa vào PTHH, tính được mol Fe phản ứng theo số mol của H2
c) Công thức tính nồng độ mol CM = n : V
Đáp án bài 6 trang 19 sgk hóa lớp 9
a) Số mol khí H2 = 3,36 : 22,4 = 0,15 mol
Phương trình phản ứng:
Fe + 2HCl → FeCl2 + H2 ↑
Phản ứng 0,15 0,3 0,15 ← 0,15 (mol)
b) Khối lượng sắt đã phản ứng:
mFe = 0,15 . 56 = 8,4 g
c) Số mol HCl phản ứng:
nHCl = 0,3 mol; 50 ml = 0,05 lít
Nồng độ mol của dung dịch HCl: 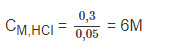
» Bài tiếp theo: Bài 7 tr 19 SGK Hóa 9